국내 연구진이 특발성 폐섬유증 치료제로 개발 중인 ‘베르시포로신(Bersiporocin)’의 작용 기전을 밝혀내 새로운 섬유증 치료제 개발에 속도가 붙을 것으로 기대된다.
연세대학교 김성훈 교수(약학대학 및 의과대학 겸임), 윤이나 박사 연구팀은 고려대학교 황광연 교수(생명공학과) 연구팀과의 공동 연구를 통해 ‘베르시포로신’의 효능과 안전성을 동시에 설명할 수 있는 분자 기전을 규명했다. 연구 결과는 5월 22일(현지 시간) 세계적인 의학 학술지 ‘EMBO 분자 의학(EMBO Molecular Medicine)’에 게재됐다.

(왼쪽부터) 연세대학교 김성훈 교수, 고려대학교 황광연 교수, 연세대학교 윤이나 박사(제1저자)
특발성 폐섬유증은 폐에 콜라겐이 비정상적으로 축적돼 폐의 기능을 상실하는 난치병으로 세계적으로 인구 10만 명당 약 13명의 빈도로 발생한다. 진단 후 5년 생존율이 40%에 불과할 정도로 예후가 좋지 않은 치명적 질환이다. 특히 기존에 허가받은 치료제들은 부작용이 심해 새로운 치료제 개발이 절실히 필요한 상황이다.
‘베르시포로신’은 콜라겐 합성을 주관하는 prolyl-tRNA synthetase 1(이하 PARS1) 효소의 활성을 억제해 치료 효과를 나타낸다. 그동안 전 세계 많은 연구자들이 PARS1의 활성 조절을 통해 섬유화증을 치료하려 했지만 PARS1이 생명 유지에 필수적인 효소이기 때문에 PARS1의 과도한 활성 억제가 자칫 부작용을 야기할 수 있어서 신약 개발에 어려움을 겪고 있었다.
따라서 치료 효과는 나타내면서도 환자에게 안전한 수준으로 PARS1의 활성을 억제하는 것이 신약 개발의 가장 큰 핵심 기술이었다.
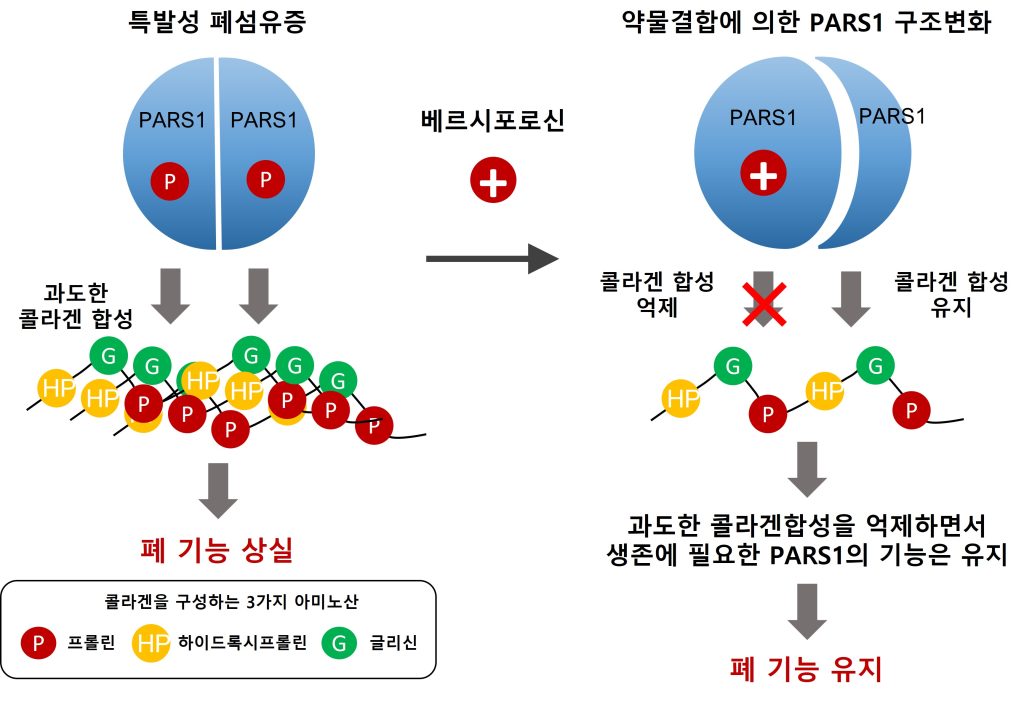
PARS1은 효소 2개가 한 쌍을 이루는 형태로 존재하는데 이번 연구를 통해 ‘베르시포로신’이 한 쌍의 효소에 비대칭적으로 결합함으로써 과도한 활성 억제를 일으키지 않아 약효를 나타내면서도 약물의 부작용을 최소화할 수 있음을 규명했다.
김성훈 교수는 “정밀 의학을 현실화하고 글로벌 수준의 신약 개발 능력을 확보하기 위해서는 새로운 기전의 신약 타깃 발굴이 절실한 상황”이라며 “이번 연구를 통해 PARS1과 같은 필수 효소들도 신약 개발을 위한 타깃으로 활용될 수 있음을 증명한 것에 큰 의미가 있다”고 강조했다.
‘베르시포로신’은 대웅제약에서 특발성 폐섬유증 치료제로 개발 중인 혁신 치료제(First-in-class)로서 2019년 미국식품의약국(FDA) 희귀 의약품으로 지정됐으며 현재 글로벌 임상 2상을 진행 중에 있다.
PARS1의 효소 활성은 콜라겐 합성을 매개해 섬유화 과정에 관여함(왼쪽). 베르시포로신이 두 개의 PARS1 중 하나와 결합하고 나면 단백질의 구조가 변화하면서 나머지 PARS1과 두 번째 약물의 결합을 방해함. 결과적으로 콜라겐 합성은 억제되지만 생명 유지에 필수적인 기능은 유지됨(오른쪽).

