(바이오스펙테이터=김성민기자) 기사입력 : 2018-10-18 13:45수정 : 2018-10-18 13:45
화학연구원-성균관대 협력, 이광호 화연 연구팀 단점이라고 여겼던 펩타이드 약물로 장내 질환 타깃해 궤양성 대장염 후보물질 검증 및 발굴…”올해 12월 임상 2a상 돌입 및 중국 임상승인신청서 제출 계획”

화학연구원과 성균관대는 함께 전임상 단계에 있는 궤양성 대장염 후보물질을 발굴해 2015년 독점 실시권을 이전했다. 올해 궤양성 대장염 환자를 대상으로 임상 2상에 돌입할 예정인 신약 후보불질이다.
“화학연구원이 개발중심 회사(NRDO, no research only development)와 첫 협력한 사례다. 브릿지바이오가 NRDO라는 점에서 기회를 봤다. 개발 중심의 바이오텍 모델이 국내 기초과학 연구자들에게 새로운 기회를 보여준다고 생각한다. 산학연이 협력해 결과를 만든 좋은 케이스로 각자 역할을 정확히 아는 것이 성공 비결이라 할 수 있겠다.”
이광호 화학연구원 박사(책임 연구원)는 혁신 신약 후보물질 ‘BBT-401(궤양성 대장염 치료제)’을 발굴한 과정을 소개했다. 그는 하버드대에서 박사후 연구원으로 있었고, 미국 노바티스에서 감염질환 분야에서 혁신신약 발굴 연구를 했다(2003~2008년). 이후 셀젠이 인수한 아빌라 테라퓨틱스(Avila therapeutics)에서 항암제 신약을 연구개발하다, 2011년 화연에 들어왔다.
브릿지바이오는 기술이전 이후 지난해 1월 BBT-401 GLP 독성시험을 시작해 올해 3월 미국 임상 돌입하며, 개발에 속도를 내고 있다. 브릿지바이오는 올해 12월 BBT-401 임상 2a상에 돌입할 예정으로 2020년 즈음 개념 입증(PoC, proof of concept) 임상 결과가 나올 것으로 예상한다. 동시에 올해 말 중국에 BBT-401 임상승인 신청서(IND filing)를 제출할 계획이다.
바이오스펙테이터는 지난 11일 대전 한국화학연구원에서 열린 ‘궤양성대장염 치료제 후보물질 BBT-401 미국 임상1상 완료 기념행사’에 참가해 과거 타깃 검증부터 임상 1상 완료까지 BBT401(TRP-401) 개발 스토리와 향후 개발 계획을 들을 수 있었다. 이번 행사는 한국화학연구원과 브릿지바이오가 공동 개최했다.
펩타이드 약물 발상의 전환, ‘장내 질환 겨낭한 BBT-401’
BBT-401은 펠리노-1 저해 약물로, 경쟁자가 없는 ‘first-in-class’ 신약 후보물질이다. BBT-401은 기초연계 신약발굴 중개 연구기관(TREND, Translational research institute for novel drug) 프로젝트에서 탄생했다. BBT-401은 이 박사 주도로 6년 동안 진행하는 TREND 프로젝트의 첫 성과다.
TREND 연구는 화연이 국내 제약 산업이 me-too 신약에서 벗어나 리스크가 큰 ‘first-in-class’ 신약 개발을 돕고자 2012년 시작했다. 화연은 국내에서 가장 큰 공공 화합물(55만 개) 라이브러리를 보유하는 등 여러 국산 신약을 발굴한 곳이다. TREND 프로젝트는 전임상 후보물질을 도출해 국내 기업에 기술 이전하는 모델로 브릿지바이오에 이어 메드팩토(면역), 동화약품(항암)에 혁신 신약 후보물질을 라이선스 아웃했다. 신촌 세브란스 병원과 발굴한 폐암 치료제 후보물질은 올해 기술이전할 목표다.
이 박사는 “혁신 신약은 새로운 사이언스에서 출발한다”며 “그럼 ‘first-in-class’ 타깃을 어떻게 찾을 수 있을까? 국내에서 나온 타깃을 가장 먼저 신약으로 개발하는 것이 관건이라고 생각했다”고 설명했다.
그렇게 주목한 것이 펠리노-1과 SMAD-6 상호 작용이었다. 2006년~2013년은 펠리노-1을 약물 표적으로 검증(target validation)한 기간으로 박석희 성균관대 교수 연구팀과 MD앤더슨 Shao-Cong Sun 교수 연구를 바탕으로 한다. MD앤더슨에서 펠리노-1 연구를 했던 장미경 박사는 현재 브릿지바이오 부사장이다.
펠리노-1은 TLR(toll-like receptor)가 매개하는 선천성 면역 작용 신호전달에 중요한 인자다. TLR 활성화되면 하위 과정에서 펠리노-1은 SMAD-6와 결합해 Myd88 복합체(complex) 혹은 RIP-1 복합체를 형성되고, 그 결과 핵 전사 인자인 NF-kB가 염증 인자 발현을 유도한다. SMAD-6는 TGF-β 하위 인자다.
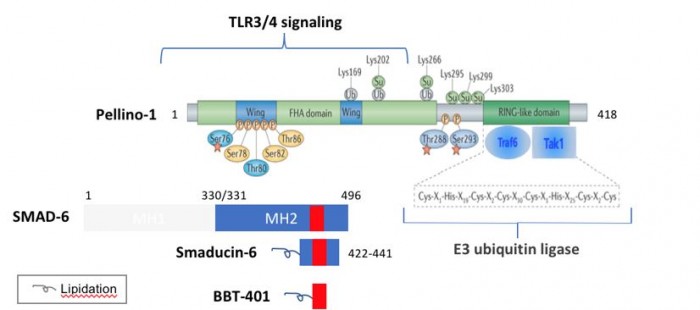
▲펠리노-1의 구조와 펠리노-1의 N말단에 결합하는 Smad6, Smaducin-6, BBT-401의 결합 부위(붉은색)
박석희 성균관대 교수 연구팀은 펠리노-1 N-말단의 1-137번 아미노산과 Smad-6 332-496번 아미노산이 결합한다는 기존 연구 결과를 바탕으로, 아미노산 서열 중 펠리노-1과 결합하는 핵심 부위를 찾아냈다. Smad-6 422-441번 아미노산이 두 단백질 상호작용에 중요했다. 연구팀은 Smad-6 20개 아미노산(422-441)에 세포막 내부로 물질을 전달하는 지방산(팔미트산)을 결합한 합성 펩타이드 물질인 스매듀신-6(Smaducin-6)를 만들었다. 박 교수 연구팀은 패혈증, 궤양성 대장염 모델에서 스매듀신-6가 항염증 작용을 한다는 것을 밝혔다.
이광호 박사 연구팀은 스매듀신-6가 가진 가능성을 봤다. 연구팀은 TREND 프로젝트 과제로 2013년부터 2년간 펠리노-1 저해제 개발 후보 발굴 연구를 진행했다.
다음 과제는 스매듀신-6를 경구 투여 약물로 만드는 일이었다. 이 박사는 “아미노산 중 활성 부위(activie site)를 찾아 크기, 합성 생산성 등 물질 최적화가 필요했다”며 “경구 투여 약물은 체내로 흡수돼 원하는 장기로 분포해야 된다. 또한 적절한 시간 동안 노출됐다 없어져야 하기 때문에 흡수, 분포, 대사 등 측면에서 이상적인 약물을 찾아야 했다”고 설명했다.
그러나 스메듀신-6과 같은 펩타이드 물질은 보통 체내에서 빠르게 대사 돼, 경구 투여 약물로 개발하기 어렵다. 이 박사도 처음에는 체내에 잘 퍼지고, 오래 유지되는 비-펩타이드(non-peptide) 약물을 찾으려고 했지만 1년 동안 시도했지만 실패했다.
이때 발상을 전환했다. 그는 “펩타이드 약물은 체내 분포가 떨어지기 때문에 특정 부위를 겨냥해야겠다고 생각했다”며 “펩타이드 약물이 가지는 단점을 장점으로 살려 장내 질환을 겨냥해 약물이 위장관에 머물도록 만들었고, 동물 실험에서 이러한 접근법이 유효한 것을 확인했다”고 설명했다. 그는 노바티스에 있을 때 장내 세균을 겨냥한 약물을 합성했을 때 물질 크기가 커 전신 노출되지 않았지만, 장에서 작용만으로도 임상에서 유효성을 확인한 예가 있었다고 부연했다. 비슷한 예도 있다. 궤양성 대장염 1차 약제인 설파살라진은 투여량의 90%가 결장(colon)에 도달해 장내 박테리아가 설파살라진을 대사한다. 대사물 중 5-ASA는 장내 머물러 항염증 작용을 해 증상을 완화한다.
연구팀은 스매듀신-6의 20개 아미노산 중 4개 아미노산을 이용해 펩타이드 약물을 디자인했다. 이후 펩타이드 서열이 약물 특성을 갖도록 최적화해 후보물질 ‘TRP-401(BBT-401)‘을 발굴했다. 약물 기전을 보면 BBT-401은 펠리노-1이 다른 단백질과 결합하는 것을 방해해 MydD88(혹은 RIP-1) 복합체 형성을 막는다. 결국 BBT-401은 NF-kB가 염증 유발 단백질을 생성하는 것을 저해해 항염증 작용을 한다.
이 박사 연구팀은 후보물질(TRP-401)을 국내 제약사에 기술이전을 하려 시도했지만 어려움에 부딪혔다. 약물이 위장관에만 머물기 때문에 제약사가 생각하는 이상적인 약물이 아니기 때문이었다는 설명. 이 박사는 “국내 제약사 20여 군데에 후보물질을 소개했지만 약물성이 없다는 이유로 얘기가 진전되지 못했다”며 “사이언스와 인더스트리, 비즈니스를 잇는 역할이 중요하다는 것을 깨달았다”고 당시 상황을 얘기했다.
이 박사는 “브릿지바이오에서 후보물질의 가치를 알아봤고, 기술이전 이후 빠르게 개발되고 있어 좋은 성공 케이스라고 생각한다”며 “바이오벤처가 특히 신약 후보물질에 더 포커스하는 경향이 있는 것 같다. BBT-401 사례는 화연뿐만 아니라 제약업계 지형에도 던지는 시사점이 크다”고 강조했다.
마지막으로 이 박사는 “최근 오픈이노베이션으로 혁신 신약을 기술이전을 하려는 움직임이 커지고 있다. 그러나 완성된 ‘first-in-class’ 신약을 찾기보단 가능성을 보고 같이 일을 해야 한다”고 강조했다. 덧붙여 그는 “처음부터 진수성찬은 없다. 밥상을 같이 만들어간다고 생각할 때 진수성찬이 될 수 있다”며 “규모가 있는 회사일수록 기초 연구자와 같이 밥상을 차린다는 생각으로 가야한다”고 말했다.
“임상 1상서 약물 전신 노출 없으며, 안전성 확인”
“BBT-401 프로젝트는 아카데미아에서 8년 동안 타깃 벨리데이션, 정부출연 연구원인 화연에서 3년간 후보물질 발굴, 이어 브릿지바이오에서 2년 6개월간 개발을 진행한 프로그램이다. 이번 달에 임상 1상이 끝났으며, 2018년 12월에 임상 2a상에 들어가는 것이 목표다.”
다음 강상욱 부사장은 BBT-401의 개발 현황 및 계획에 대해 발표했다. 강 부사장은 CMC와 의약화학(medicinal chemistry) 파트를 담당한다. 면역질환 모델에서 펠리노-1 타깃 벨리데이션 연구를 진행했던 장미경 박사는 2016년, 박석희 교수팀의 이연숙 박사는 지난해 브릿지바이오에 합류했다.
타깃 질환인 궤양성대장염은 대표적인 염증질환으로 대장의 끝부분에서 만성염증으로 인한 궤양이 발생해 혈변, 잦은 설사, 복부 통증 등으로 일상적인 생활에 지장을 준다. 강 부사장은 “1~3차 약제이 있지만, 아직 미충족 수요가 높은 질환이다”고 말했다.
1차약제로 70% 환자에 5-ASA(펜티사, 아시콜)가 투약되며 완전 관해율은 20%, 반응률은 50%다. 5-ASA가 듣지 않는 환자에 2차 약제로 단기적으로 스테로이드를 처방하지만 부작용 문제가 있다. 3차 약제로는 항 TNF-α 항체(ex. 엔브렐, 휴미라), 항 IL-12/IL-23 항체 ‘우수테키누맙(스텔라라)’ 등을 처방된다. 항체 약물은 반응률이 80%로 높은 수치를 보이지만, 가격이 비싸다. BBT-401은 기존 약제와 비교했을 때 약물 효능, 안전성 면에서 우수하다고 소개했다.
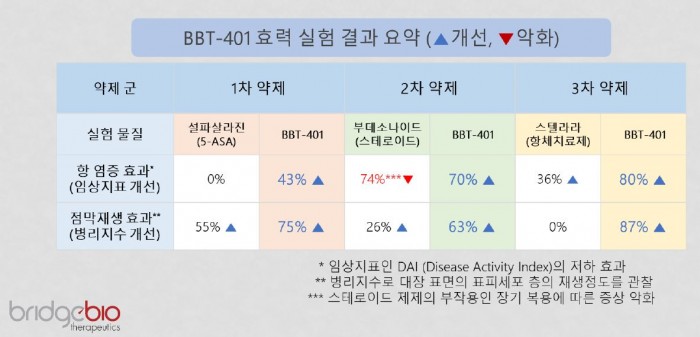
▲동물 모델에서 약물 효능 테스트를 한 결과를 표로 나타냈다.
먼저 유효성 데이터를 보면 강 부사장은 “전임상 결과를 보면 경쟁 약물군과 비교해 우수한 항염증 효과와 점막재생 효과가 있었다”고 강조했다. 동물 실험을 CRO에 위탁해 진행했다. 약물 효능을 테스트한 결과 1차 약제인 5-ASA는 점막재생 효과가 있지만, 항염증 효과는 없었다. 2차 약제인 스테로이드 약물은 부작용 문제가 있었으며, 3차 약제인 항체 약물은 항염증 효과가 있으나 점막 재생 효과는 없었다는 설명이다.
강 부사장은 “다음 효능에 이어 경쟁 제품 대비 우수한 안전성 확인했다”며 “임상 1상에 일반인 피험자에 약물을 투여한 결과 심각한 부작용(SAEs)은 없었으며, 다중용량상승시험(MAD)에서 7일 동안 1회/1일로 최대 1.6g까지 경구투약했다”며 “예상대로 약물 전신 노출은 없었다”고 설명했다.
올해 12월 중에 국가식품의약품관리감독총국(CFDA)에 임상승인 신청서를 제출할 예정이다. 강 부사장은 “향후 선진국 개발은 글로벌 파트너와 협력해 진행할 예정”이라며 “중국을 포함한 다른 국가는 지역 파트너와 글로벌 파트너를 중계해 개발하는 전략”이라고 설명했다.
브릿지바이오는 안과 질환, 상기도 호흡기 질환 및 피부질환 등 여러 질환에서 항염증 신호 전달 및 면역 조절 기전 변화를 통한 BBT-401의 치료 효능을 테스트하고 있다.

원문: http://biospectator.com/view/news_view.php?varAtcId=6346
