(메디게이트뉴스=박도영 기자) 기사입력시간 18.10.11 06:27 | 최종 업데이트 18.10.11 06:27
[ESMO 2018] 셀리드·종근당·GC녹십자 등 신약 임상결과 발표
올해 유럽종양학회 연례학술대회(ESMO 2018)에서는 국산 항암 신약 4개에 대한 초록이 발표될 것으로 전망된다.
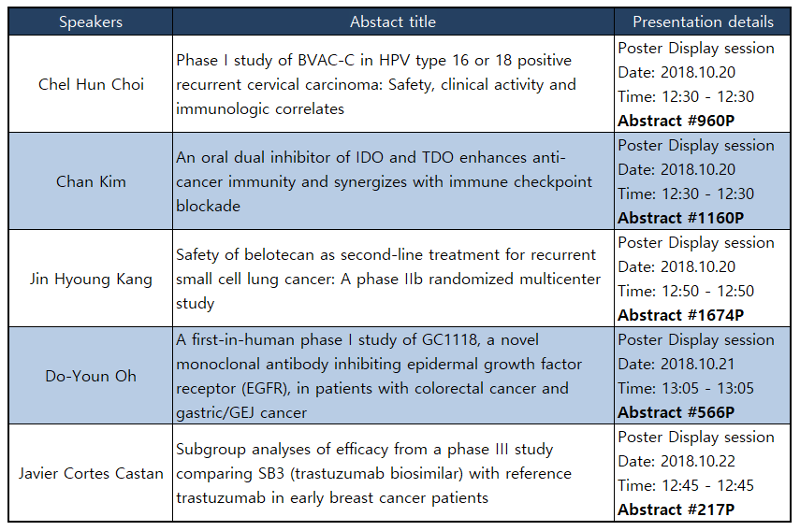
유럽종양학회는 9일(현지시간) 연례학술대회에서 발표될 포스터 초록을 공개했다. 본지에서 확인한 결과 국산 신약으로는 셀리드의 BVAC-C, 종간당의 캄토벨, GC녹십자의 GC1118 임상 결과가 발표되며, 초기 데이터지만 분당차병원 연구팀의 IDO·TDO 이중 억제 경구제 후보물질에 대한 데이터도 소개된다. 국산 바이오시밀러(biosimilar) 관련 연구로는 삼성바이오에피스의 온트루잔트 효능 하위분석 결과가 나온다.
셀리드 자궁경부암 치료제 BVAC-C 1상 결과는
세포 기반 항암면역치료백신 개발 기업인 셀리드(Cellid)는 자궁경부암 치료 후보물질인 BVAC-C의 1상 임상 결과를 발표한다.
셀리드가 개발하고 있는 치료백신은 환자 자신의 B세포(B lynphocytes)와 단구(Monocytes)를 항원제시세포로 활용하고, 유전자, 단백질, 펩타이드 형태의 암 항원을 적재한 뒤 자연살해 T세포(Natural Killer T cells) 리간드인 알파-갈락토실세라마이드(α-galactosylceramide)를 면역증강제로 첨가한 형태다.
BVAC-C는 아데노바이러스 백터를 이용해 전달하며, 인유두종 바이러스(HPV) 16·18형 발암유전자인 E6·E7유전자를 재조합한 암항원 유전자를 사용해 면역반응을 유도한다. 자궁경부암 에방백신이 HPV 표면 단백질 L1, L2을 사용해 감염 전에만 효과를 발휘한다면, BVAC-C는 발암 이후 자궁경부암의 치료에 사용할 수 있다.
1상 임상에서는 최소 1회 백금 기반 병용 항암화학요법으로 치료받은 뒤 재발한 HPV 16형 또는 18형 양성 환자 10명을 대상으로 진행됐다. 연구 결과 BVAC-C는 HPV 16 또는 18형 자궁경부암에 내약성이 뛰어나고 항암활성의 근거와도 연관성이 있는 것으로 나타났다.
BVAC-C는 현재 2a상 임상을 진행하고 있으며, 2021년 바이오신약 허가신청(Biologics License Application, BLA)을 목표로 개발하고 있다.
분당차병원 연구팀, IDO·TDO 이중 억제제 초기결과 발표
분당차병원 종양내과 김찬 교수는 IDO(Indolamine 2,3-dioxygenase)와 TDO(Trp 2,3-dioxygenase)를 이중으로 억제하는 경구 후보물질인 CB548에 대한 연구결과를 발표한다.
IDO 억제제는 기대되는 후보물질이었으나 최근 실패 소식이 연이어 전해지고 있다. 가장 촉망받는 후보물질이었던 인사이트(Incyte)의 에파카도스타트(epacadostat)는 올해 4월 키트루다(Keytruda, 성분명 펨브롤리주맙)와의 병용 임상시험에서 무진행 생존기간을 개선시키지 못했다. 같은달 BMS는 BMS-986205와 옵디보(Opdivo, 성분명 니볼루맙) 병용요법에 대한 3상 임상시험 2건을 중단했고, 로슈 제넨텍(Genentech)은 5월 뉴링크 제네틱스(NewLink Geneteics)와 IDO-TDO- 억제제 연구 제휴를 중단했다.
김 교수팀은 이번에 발표하는 연구에서 IDO와 TDO를 위한 저분자 억제제를 합성하고, 인비트로(in vitro) IDO/TDO 효소 및 세포 기반 검사(assays)를 통해 스크리닝했다. 또한 리드 화합물(lead compound)인 CB548 단독 또는 항-PD1 항체와의 병용으로 CT26 결장 또는 4T1 유방 종양을 가지고 있는 마우스를 치료했다.
연구 결과 IDO/TDO 이중 억제제인 CB548은 강력한 항암 면역을 유도하고, 면역관문억제제와의 병용으로 암 진행 억제에 시너지 효과를 내는 것으로 나타났다.
종근당, 세계폐암학회 이어 캄토벨 안전성 데이터 공개
종근당(Chong Kun Dang)의 캄토벨(성분명 벨로테칸)에 대한 2b상 임상 결과도 발표된다.
종근당은 2010년 2월부터 2018년 3월까지 약 8년에 걸쳐 국립암센터를 비롯한 전국 13개 기관에서 소세포폐암 재발 환자 164명을 대상으로 캄토벨과 토포테칸의 유효성과 안전성을 비교평가 하는 후기 임상 2상 시험을 진행했다.
9월 캐나다 토론토에서 열린 세계폐암학회(WCLC 2018)에서는 캄토벨의 유효성 결과를 발표했다. 발표에서 캄토벨의 객관적 반응율(Objective Response Rate)은 36.33%로 비교약물인 토포테칸 21.05%과 비열등했고, 전체 생존(Overall Survival) 기간은 유의하게 연장시켰다.
이번 학회에서는 캄토벨의 안전성 데이터를 공개할 예정이다.
이번 임상으로 종근당은 확증 임상시험의 조건부로 허가 받은 국내 항암제 신약 중 처음으로 소세포폐암과 난소암 2개 적응증에 대한 비교 임상시험을 통해 유효성과 안전성을 입증하게 됐다.
GC녹십자 GC1118의 대장암·위암 데이터
GC녹십자는 신규 항-EGFR 단일클론항체인 GC1118의 1상 임상 결과를 발표한다.
GC1118은 앞서 출시한 다국적 제약사의 EGFR 표적치료제들 대비 차별적인 결합방식과 작용기전을 가진 바이오 신약으로, 다양한 종류의 EGFR 리간드에 억제효과를 보이는 것이 특징이다. 기존 EGFR항체 대비 차별적인 효능을 보일 것으로 예측되며, KRAS 변이 모델에서 기존 항체보다 종양억제효과가 우수할 것으로 기대된다.
고형암 환자를 대상으로 한 1상 임상 용량증량시험이 완료됐으며, 이번 학회에서는 대장암 및 위암 환자에서 효능 및 안전성 데이터를 발표한다.
코호트 1에는 5-플루오로우라실(5-FU), 옥살리플라틴(oxaliplatin), 이리노테칸(irinotecan) 치료에 실패한 EGFR 항체 치료 경험이 없는 전이성 대장암 환자, 코호트 2에는 이전 EGFR 치료에 저항성을 보인 전이성 대장암 환자, 코호트 3에는 표준 치료에 실패한 EGFR 과발현 전이성 위암 환자가 등록됐다.
이 연구에서 GC1118은 유망한 항종양 활성을 나타냈고, 내약성이 좋았고, 가장 흔한 이상 반응은 피부 독성이었다.
이 외에도 삼성바이오에피스(Samsung Bioepis)의 허셉틴(Herceptin, 성분명 트라스투주맙) 바이오시밀러(biosimilar)인 온트루잔트(Ontruzant, 개발명 SB3)에 대한 새로운 데이터도 발표된다.
이번 발표에서는 오리지널 의약품과 비교한 3상임상에서 대상자들의 기저 질환 및 인구학적 특성 별 하위그룹에 따른 효능 분석 결과를 공개한다.
한편 올해 유럽종양학회 연례학술대회는 19~23일(현지시간) 독일 뮌헨에서 열리며, 전 세계에서 2만여 명의 종양학 전문가들이 참석할 예정이다.
